GLP-1は、小腸から分泌されるホルモンであり、食後の血糖値をコントロールする作用を持ちます。
GLP -1と同様の働きをするGLP-1受容体作動薬(グルカゴン様ペプチド-1受容体作動薬)は、主に2型糖尿病に使用される薬剤です。
GLP-1受容体作動薬は、体の自然な生理的機能に近い形で作用するため、血糖値のコントロールを副作用のリスクを抑えて実現できる設計になっています。
そのため、現在は肥満症の薬物療法やにも使用されている治療薬です。
手に取りやすい薬となっている反面、作用機序・適正使用について理解が浅い状態で使用する方が増えているため、
当記事では糖尿病を含む内科疾患全般の診療に従事している医師の監修の下、GLP-1受容体作動薬について詳細に解説していきます。
GLP-1受容体作動薬の作用機序【医師監修】
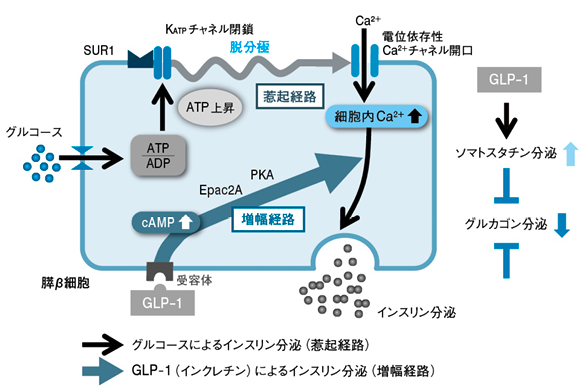
引用:日本医事新報社
GLP-1受容体作動薬は、非常に明確な作用機序を持っています。
体内の自然なホルモンであるGLP-1(グルカゴン様ペプチド-1)の働きを模倣することで、主に
・インスリン分泌の促進
・グルカゴン分泌の抑制
・胃排出の遅延
・中枢神経への作用
などの作用があります。
この作用機序は、数多くの臨床試験や研究で効果が確認されています。
特に、糖尿病患者における血糖コントロールの改善や体重減少の効果が科学的に証明されています。
また、GLP-1受容体作動薬は心血管疾患のリスクを低下させる可能性・炎症性筋疾患モデルを改善させる可能性があることも報告されており、今後も幅広い用法が期待されています。
GLP-1受容体作動薬の作用機序① インスリン分泌の促進
GLP-1受容体作動薬は、小膵臓のβ細胞に作用してインスリンの分泌を促進する作用を持ちます。
このような作用を持つホルモンは、「インクレチン」と定義されています。
GLP-1は、インクレチンと呼ばれる消化管ホルモンの一種で、食後の血糖コントロールに関与します。インクレチンには、膵臓のβ細胞を刺激して血糖依存的にインスリン分泌を促進する作用があり、この“インクレチン効果”がGLP-1受容体作動薬の血糖管理に寄与しています。また、GLP-1は短い半減期(血中半減期は約2分)を持つため、GLP-1受容体作動薬はGLP-1ホルモンを分解する酵素「DPP-4」に対する抵抗性を持つように設計されています。また、分子構造を改変して体内での安定性を高めたり、持続性を持たせるために徐放性製剤として開発されています。
参考:公益財団法人 腸内細菌学会・日医NEWS ONLINE
食事に伴って血糖値が上昇したときに作用して、インスリン分泌を増加させます。
血糖値が低いときにはインスリン分泌の作用を起こさないため、低血糖のリスクが比較的少ないのが特徴です。
インスリンは肝臓・筋肉・脂肪組織の細胞に作用して、血液中のグルコースを細胞に取り込ませます。
他にも、肝臓に作用して余分なグルコースをグリコーゲンとして貯蓄します。(グリコーゲン合成)
また、インスリンは肝臓での糖新生(グルコースの産生)を抑制するため、血糖値が過度に上昇しないようにコントロールします。
このように、インスリンは複数の働きにより血糖値を制御することができるホルモンです。
GLP-1受容体作動薬の作用機序② グルカゴン分泌の抑制
GLP-1は膵臓のα細胞に作用して、血糖を上昇させるホルモンであるグルカゴンの分泌を抑制します。
肝臓でのグリコーゲン分解や糖新生が抑制されるため、空腹時の血糖値の上昇を防ぐことができます。
また、GLP-1が膵島(ランゲルハンス島)のβ細胞やδ細胞に作用すると、インスリンやソマトスタチンなどのグルカゴンに対する抑制因子が分泌されます。
これは、先述したα細胞への直接的な作用よりも強い抑制作用があります。
GLP-1受容体作動薬の作用機序③ 胃排出の遅延
GLP-1受容体作動薬は、胃の排出を遅延させることで食後の血糖値の上昇を抑えます。
まず、GLP-1受容体作動薬は胃の平滑筋に作用し、その収縮を抑えることで胃を弛緩させます。
この作用により、胃内にある食物が小腸へ移動する速度が遅くなり、消化・吸収が緩やかに進行します。
特に、胃の出口付近にある胃前庭部の蠕動運動が抑えられるため、食物が胃に留まる時間が長くなります。
さらに、幽門括約筋(胃と小腸をつなぐ筋肉)の収縮が促され、胃内容物の小腸への排出が物理的に制限されます。
GLP-1受容体作動薬の作用機序④ 中枢神経への作用による満腹感
GLP-1受容体作動薬は中枢神経に作用して満腹感を高め、食欲を抑制します。
満腹感に対して「直接的・間接的」な作用を持っており、主に4つの働きによって満腹感はもたらされるので、それぞれ解説します。
迷走神経を介した信号伝達
GLP-1受容体作動薬は、消化管から迷走神経を介して中枢神経系に信号を送ります。
迷走神経の求心性線維が刺激されると、この信号は延髄の孤束核に伝えられる後に、視床下部へと伝達されます。
視床下部は体内のエネルギー調節を行う中心であり、この信号により「満腹感」を感じさせる指令が脳全体に送られます。
視床下部への直接作用
GLP-1は血液脳関門を一部通過することができ、直接的に視床下部に存在するGLP-1受容体に作用します。
視床下部の弓状核・室傍核・視索上核などの部位に作用することで、食欲抑制ホルモンの放出を促進します。
神経伝達物質の調節
GLP-1受容体作動薬は、ドーパミンやセロトニンなどの神経伝達物質の放出にも影響を与えることが示されています。
これにより、食後の満足感が得られやすくなると共に食事後の満腹感が強化されます。
胃排出遅延との相乗効果
GLP-1受容体作動薬は迷走神経を介して中枢神経系に信号を送り、胃の運動をさらに抑えるように調整します。
これにより、神経系を通じた消化管運動の抑制が行われ、胃排出が遅延する効果が発揮されます。
食後の糖質吸収を緩やかにすることで血糖値の急上昇を防ぐだけでなく、食後も胃内に食物が留まることで満腹感が持続します。
GLP-1受容体作動薬の適正使用について【医師監修】
GLP-1受容体作動薬(GLP-1RA)は、主に2型糖尿病の治療において重要な役割を果たし、特に肥満を伴う患者においては体重減少効果も期待されています。
しかし、近年、美容目的での適応外使用によるリスクが問題視されています。
しかし、適正に使用しなければ思わぬ副作用のリスクがあり、適応外使用は大きな健康被害を招く可能性があるため、医師の指導のもと使用するようにしてください。
ここからは、GLP-1受容体作動薬の適正使用について、具体的な注意事項を説明します。
GLP-1受容体作動薬の適正使用① 適応患者の選定
GLP-1受容体作動薬は、2型糖尿病患者で血糖コントロールが不十分な場合に用いられます。
特に肥満を伴う患者では、体重減少の効果も期待されますが、医療用としての使用は承認されていません。
適正使用が求められる理由は、薬剤の本来の効果を安全に引き出すためです。
一方で医師が法律に基づいて自由診療における適応外使用(オフラベル使用)を行うこと自体は禁止されていません。
ただし、その場合には科学的根拠を持って患者にメリットとリスクを十分に説明し、インフォームド・コンセントを得る必要があります。
 編集部
編集部トラブルの原因になるので、納得してから治療を受けるようにしてください。
美容目的で処方されているケースはこの自由診療の範囲内で行われているので、処方を受ける場合は必ず医師の説明を受けてください。
肥満症患者におけるGLP-1受容体作動薬の適用基準
| 項目 | 条件 |
|---|---|
| 肥満症の定義 | BMI 25kg/m²以上で脂肪が過剰に蓄積し、肥満に起因または関連する健康障害を合併する、またはその合併が予測される疾患。 |
| 適応となるBMI | 1. BMI 27kg/m²以上かつ2つ以上の肥満に関連する健康障害を有する場合 2. BMI 35kg/m²以上で、高血圧、脂質異常症、または2型糖尿病のいずれかを有する場合 |
| 必須の健康障害 | 高血圧、脂質異常症、2型糖尿病のいずれかを有し、さらに以下の11の健康障害のうち1つ以上を合併していること 1. 耐糖能障害 2. 脂質異常症 3. 高血圧 4. 高尿酸血症・痛風 5. 冠動脈疾患 6. 脳梗塞・一過性脳虚血発作 7. 非アルコール性脂肪性肝疾患 8. 月経異常・女性不妊 9. 閉塞性睡眠時無呼吸症候群・肥満低換気症候群 10. 運動器疾患(変形性関節症、変形性脊椎症など) 11. 肥満関連腎臓病 |
| 適応の前提条件 | 1. 食事療法、運動療法、行動療法を実施しても十分な効果が得られなかった場合に限り、薬物治療を考慮する。 2. 内分泌性肥満、遺伝性肥満、視床下部性肥満、薬剤性肥満などの二次性肥満の場合は、まず原因精査と原疾患の治療を優先。 |
| その他の注意事項 | 使用時は、糖尿病を併発している場合、他の血糖降下薬と併用する際の低血糖リスクに注意。メンタルヘルスにも配慮し、甲状腺髄様癌の既往がある場合には慎重に対応する。 |
GLP-1受容体作動薬の適正使用② 投与量と頻度などの管理
一人ひとりの個人差に応じて適切な初期投与量を設定した上で、効果・副作用を考慮しながら徐々に投与量を増量して体に適応させます(漸増投与)。
初期投与量は、血糖コントロール状況・体重・年齢・既往歴などをもとに決定されます。
注射薬・内服薬によって服薬の周期は週1回の投与・1日1回の投与に分かれる場合もあるため、医師の指導に従って使用する必要があります。
また、投与中も定期的に血糖値や体重を測定して、副作用が大きい場合は投薬を中止する選択肢も検討されます。
GLP-1受容体作動薬の適正使用③ 併用療法と食事・運動管理
インスリンやスルホニルウレア薬などの他の糖尿病治療薬と併用する場合は低血糖のリスクが非常に高まるため、注意が必要であり医師の管理が必要になります。
また、生活習慣の改善と並行して行うことで、治療効果が最大限に発揮されるとともに、服薬終了後も健康な体を維持することができます。
そのため、食事療法や適度な運動を行いながら服薬することでより高い効果を発揮します。
GLP-1受容体作動薬の適正使用④ 副作用とリスク管理
一般的な副作用には、以下のような内容が挙げられます。
・低血糖(特に糖尿病治療薬と併用時に危険)
・消化器症状(吐き気・下痢・便秘・腹痛)
・急性膵炎(持続的な激しい腹痛を伴う)
・重篤なリスク(腸閉塞・腎不全・アナフィラキシー)
重篤な副作用として膵炎や腸閉塞のリスクがあるため、これらの症状が現れた場合は直ちに服薬をやめてすぐに医療機関に相談する必要があります。
GLP-1受容体作動薬の適正使用⑤ 特定の患者に対する使用の注意点
GLP-1受容体作動薬は、特定の甲状腺疾患や膵炎の既往歴がある患者には使用が禁忌とされています。
また、妊娠中や授乳中の使用は医師の管理のもと慎重に行う必要があります。
2.禁忌(次の患者には投与しないこと)
2.1 本剤の成分に対し過敏症の既往歴のある患者
2.2 糖尿病性ケトアシドーシス、糖尿病性昏睡又は前昏睡、1型糖尿病の患者[インスリン製剤による速やかな治療が必須となるので、本剤を投与すべきでない。]
2.3 重症感染症、手術等の緊急の場合[インスリン製剤による血糖管理が望まれるので、本剤の投与は適さない。]
引用:医療用医薬品 : オゼンピック
GLP-1受容体作動薬の効果に関する研究での効果の裏付け
GLP-1受容体作動薬の効果に関する研究① 血糖コントロールの改善効果
多くの臨床研究において、GLP-1受容体作動薬は2型糖尿病患者の血糖値を効果的に改善することが示されています。GLP-1受容体作動薬は、食後の高血糖を抑え、空腹時血糖値の低下にも寄与します。
例えば、大規模臨床試験では、HbA1c(糖化ヘモグロビン)の平均値が使用開始から6か月で0.8〜1.5%の減少を示し、多くの患者で血糖値の目標達成率が向上しました。
GLP-1受容体作動薬の効果に関する研究② 体重減少への効果
GLP-1受容体作動薬は食欲抑制効果を持ち、体重管理にも有用です。食事量の自然な減少や満腹感の持続によって、体重減少が期待されます。複数の研究により、治療を開始してから数か月で平均2〜5kgの体重減少が確認されています。
特に肥満を伴う2型糖尿病患者では、体重減少が血糖コントロールの改善にも寄与し、総合的な健康改善が報告されています。
GLP-1受容体作動薬の効果に関する研究③ 心血管リスクの低減
GLP-1受容体作動薬は、特定の薬剤において心血管疾患のリスク低減効果が確認されています。心血管アウトカム試験(CVOT)では、心筋梗塞、脳卒中、心血管死などの重大な心血管イベントの発生率が有意に低下したことが報告されています。
ある研究では、2型糖尿病および高リスクの心血管疾患を有する患者において、GLP-1受容体作動薬が心血管死亡率を15%まで低下させる結果が得られました。このデータは心血管リスクの高い患者にとっての重要な治療選択肢であることを示しています。
GLP-1受容体作動薬の効果に関する研究④ 膵臓への影響と安全性の評価
GLP-1受容体作動薬に関する安全性研究では、膵炎や腫瘍リスクの懸念も挙げられていますが、これまでの多くの臨床試験では重篤なリスクの発生率は低いことが示されています。
長期的な安全性に関しても、膵臓への影響が特に問題とされる患者においては慎重なモニタリングが推奨されていますが、現時点でのエビデンスは、適切な使用により安全性が確保されるとされています。
GLP-1受容体作動薬の効果に関する研究⑤ 患者の満足度と生活の質の向上
GLP-1受容体作動薬は血糖コントロールの改善と体重減少を通じて、患者の生活の質(QOL)を向上させる効果があるとされています。
研究によれば、治療を受けた患者の多くが自己管理への自信を持つようになり、体重や血糖値の改善によって精神的な満足度が高まることが報告されています。
さらに、注射頻度が少ない製剤・内服薬なども登場し、患者の治療負担が軽減されることで継続しやすい治療法として評価されています。
GLP-1受容体作動薬の研究の変遷
GLP-1受容体作動薬は、2型糖尿病の治療において革命的な役割を果たしています。
ここからは、インクレチン研究の歴史を辿りながら、GLP-1に基づく治療がどのように誕生し、進化してきたかを詳しく解説します。
糖尿病治療の歴史・背景を知ることで、GLP-1受容体作動薬の重要性をより一層理解することができます。
GLP-1受容体作動薬の研究の変遷① インクレチンの発見研究の始まり(1900~1960年代)
インクレチンの概念と研究の歴史は、1902年にBaylissとStarlingが発見した「セクレチン」にさかのぼります。
腸管が膵内分泌機能を調節する物質を持つことが示唆され、1932年に「インクレチン」という名前が誕生しました。
また、1960年代にインスリンの放射免疫測定(RIA)が開発され、インクレチン研究が復活し、経口ブドウ糖が静脈注射よりも多くインスリンを分泌する「インクレチン効果」が確認されました。
GLP-1受容体作動薬の研究の変遷② GLP-1の効果の解明と臨床応用(1980年代)
1980年代は、GLP-1(グルカゴン様ペプチド-1)の生理的作用が解明され、2型糖尿病治療に革新をもたらした時代です。
ジョエル・F・ハベナー(Joel F. Habener)氏・スヴェトラーナ・モジョフ(Svetlana Mojsov)氏・イェンス・ジュール・ホルスト(Jens Juul Holst)氏という3人の研究者の貢献が大きく、彼らの研究により、GLP-1(7-37)が発見されています。
彼らはGLP-1の発見の功績により、2024年に「唐奨」のバイオ医薬賞を受賞しました。
参考:2024 Tang Prize Laureates Announced: Six Global Visionaries to Be Honored in Taiwan This September

この時期、インスリン分泌のメカニズムやGLP-1の生理的役割の理解が深まり、GLP-1をベースとした治療薬の開発が加速しました。
食欲抑制や体重減少にも寄与することが分かり、肥満治療への応用も進んでいる点も重要です。
DPP-4酵素によるGLP-1の分解を防ぐ技術が進化し、持続効果を持つ薬剤が実用化される土台が築かれました
GLP-1受容体作動薬の研究の変遷③ 最初のGLP-1受容体作動薬の承認(2005年)
2005年、世界初のGLP-1受容体作動薬「エキセナチド」が米国でFDAの承認を受けました。

この薬は1日2回の皮下注射として投与されます。
体内にある自然のGLP-1と同様の作用を持ちつつ、DPP-4酵素による分解を遅らせることで持続的な効果を発揮します。
GLP-1受容体作動薬の研究の変遷④ 新たな薬剤の開発と改良(2010年代~現在)
その後、より持続時間の長い薬剤(オゼンピックなどの週1回の注射が可能な薬)が登場し、副作用の軽減や効果の向上に成功しました。
その後、日本ではノボノルディスク ファーマにより、2021年2月5日に経口GLP-1受容体作動薬「リベルサス錠」が発売されました。
世界初にして唯一の経口投与可能なGLP-1受容体作動薬であり、これまでのGLP-1受容体作動薬は注射剤しかなかったため、患者にとって負担が大きいという課題を解決する治療法になりました。
「リベルサス錠」の経口化を実現するためには、ペプチド医薬であるセマグルチドが消化管での分解を受けやすいという課題を克服する必要がありました。
ノボノルディスクは、吸収促進剤SNAC(サルカプロザートナトリウム)を使用し、胃内での分解からセマグルチドを保護し、上皮細胞への透過性を高めることで経口投与を可能にしました。
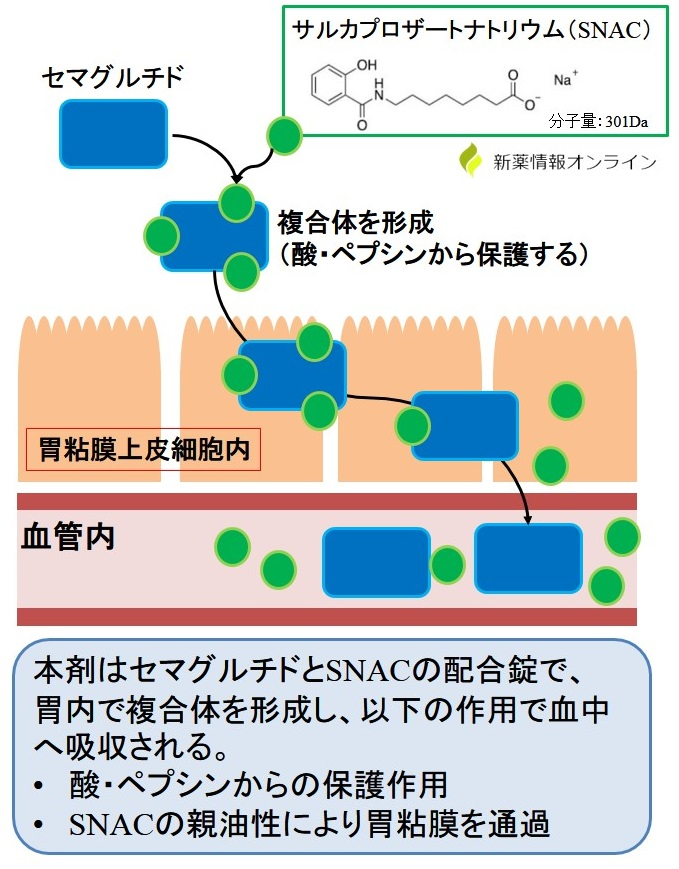
引用:リベルサス(経口のセマグルチド)の作用機序と特徴【糖尿病】
この薬剤は、PIONEER試験プログラムに基づいて承認されました。日本人を含む9,543人の2型糖尿病患者を対象とした臨床試験で、「リベルサス錠」7mgと14mgは、他の治療薬と比較して有意なHbA1cの低下を示しました。
臨床試験データ概要: 26週間後のHbA1c低下量
| 投与群 | HbA1c 基準値 (%) | HbA1c 低下量 (%) | サンプルサイズ (n) |
|---|---|---|---|
| リベルサス 3mg | 7.9 ± 0.7 | -0.9 ± 1.2 | 167 |
| リベルサス 7mg | 8.0 ± 0.6 | -1.3 ± 1.0 | 160 |
| リベルサス 14mg | 8.0 ± 0.7 | -1.5 ± 1.0 | 160 |
| プラセボ | 7.9 ± 0.7 | -0.3 ± 1.2 | 168 |
リベルサスのすべての投与量は、プラセボ群と比較して統計的に有意なHbA1cの低下を示した (p < 0.0001)ため、統計的優位性があると判断されている。





